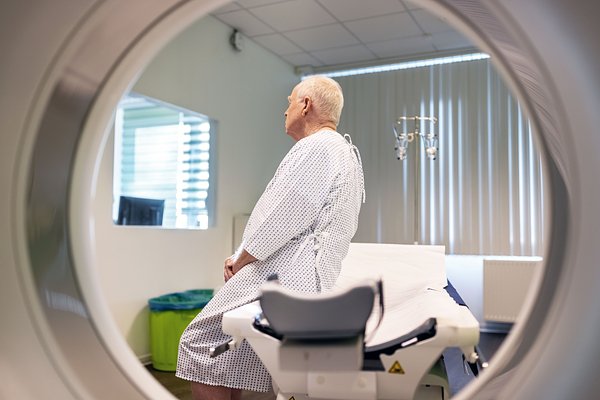
В ближайшее время в России начнутся клинические испытания вакцины против рака. Ученые надеются, что этот препарат значительно увеличит продолжительность жизни пациентов с онкологическими заболеваниями и поможет избежать рецидивов. Как будет применяться препарат и в каких случаях он может оказаться эффективным, «Ленте.ру» рассказал один из разработчиков вакцины, директор научно-исследовательского института экспериментальной диагностики и терапии опухолей Национального медицинского исследовательского центра онкологии имени Н.Н. Блохина, кандидат биологических наук Вячеслав Косоруков.
«Лента.ру»: На какой стадии сейчас разработка вакцины от рака?
Вячеслав Косоруков: В настоящее время в нашей стране ведется работа по созданию нескольких вариантов вакцины от рака, в том числе клеточной. Но вы, скорее всего, говорите об мРНК-вакцине, в разработке которой участвуют несколько институтов — НМИЦ онкологии имени Н.Н. Блохина, НМИЦ радиологии имени П.А. Герцена, НИЦЭМ имени Н.Ф. Гамалеи. Также в «Сириусе» есть лаборатория, которая ведет основные исследования в этой области. Это своего рода консорциум, который занимается разработкой в этом направлении.
Большая часть работы уже выполнена. Клинические исследования, вероятно, начнутся в ближайшее время. Они могут быть либо полноценными клиническими испытаниями, либо так называемыми исследованиями в рамках клинических исключений
С нового года в России появится нормативная база, позволяющая использовать персонализированные препараты для лечения пациентов в исключительных случаях, когда, например, еще невозможно провести полноценные клинические исследования. Наша вакцина — это как раз такой препарат. Она будет создаваться индивидуально для каждого пациента на основе его генома и генома его опухоли. После операции такая вакцина будет выполнять роль лекарственного средства, то есть станет терапевтической вакциной.
То есть с нового года вы сможете одновременно проводить исследования и оказывать медицинскую помощь?
Надеюсь, что мы сможем завершить все необходимые процедуры регистрации и получить разрешение на практическое применение этой технологии на площадках НМИЦ онкологии имени Н.Н. Блохина и НМИЦ радиологии имени П.А. Герцена в ближайшее время.

Фото: Maxim Shemetov / Reuters
Вакцина подходит для всех видов раков?
Важно понимать, что это вовсе не панацея. Прочитав заголовки в прессе, некоторые думают, что речь идет о чудодейственном средстве, которое может вылечить все. Однако это не так.
Вакцина будет эффективна только при определенных видах рака, для которых показано применение иммунотерапии. Сейчас существуют клинические рекомендации, в которых указано, где и когда можно использовать иммунотерапию.
Пока это ограниченный список заболеваний — например, меланома. В будущем туда могут войти рак легкого, некоторые виды рака ЖКТ и, возможно, рак почки. Для каждого из этих видов рака необходимо провести отдельные испытания, чтобы подтвердить эффективность вакцины. Это большая работа, которую мы планируем выполнить в кратчайшие сроки
Сможет ли вакцина от меланомы или вакцина от рака почки помочь каждому пациенту с этими заболеваниями или для кого-то она окажется бесполезной? Можно ли заранее узнать об этом?
Помимо разработки самой вакцины, создается специальная диагностическая платформа. Она будет анализировать данные о пациентах и давать рекомендации относительно эффективности применения вакцины.
Опухоль у некоторых пациентов накапливает мутации, из-за чего ее клетки начинают сильно отличаться от нормальных клеток. В частности, измененные белки немного отличаются от нормальных. Диагностическая платформа поможет обнаружить эти изменения и обучить иммунную систему распознавать их. Именно на этом принципе и основана возможность применения вакцины.
Чтобы вакцина была эффективной, необходимо значительное количество изменений в геноме опухоли, например, сотни. Из них можно выбрать 20-30 наиболее эффективных мутаций, так называемых неоантигенов, которые позволят обучить иммунную систему распознавать и атаковать опухоль.
Если у пациента мало изменений в геноме опухоли, то вакцина может оказаться неэффективной. Это связано с тем, что отличий от нормальной ткани мало, и иммунная система может не распознать опухоль как угрозу.
А много таких случаев?
Опухоли могут развиваться по разным сценариям. Иногда они накапливают мутации, а иногда происходят точечные мутации в драйверных генах. Также может быть наследственная предрасположенность к развитию опухоли. Существует более трехсот различных вариантов опухолей, каждый из них может иметь свои вариации по степени агрессивности, мутационной нагрузке и другим параметрам.
При выборе терапии, основанной на вакцине, мы будем ориентироваться на пациентов, которые могут положительно отреагировать на лечение. Кроме того, важную роль играет состояние иммунной системы человека и то, как она взаимодействует с опухолью. В некоторых случаях может потребоваться применение дополнительных методов, таких как терапия ингибиторами контрольных точек или использование антител, которые помогают иммунной системе распознавать и атаковать опухоль.
«Появляются клоны опухоли»
Как будет вакцина «готовиться»?
Для получения первого этапа и персональных маркеров вакцины нам необходимо получить опухоль прямо во время операции. Хотя ее количество может быть небольшим — всего несколько сотен миллиграммов, — она должна быть свежей, чтобы результаты были достоверными.
Это связано с тем, что для получения данных нам нужен транскриптом — набор РНК, который присутствует в опухоли в данный момент. Этот набор позволяет определить, какие белки синтезируются в опухоли.
Затем мы синтезируем норму экзома генома пациента и экзома опухоли — тех белков, которые обычно отличают опухоль от нормы. С помощью специальных инструментов мы выбираем последовательность, которой никогда раньше не было в организме. Последовательности неоантигенов будут объединены в кассету и синтезированы в форме мРНК.
Именно эта работа и нюансы, связанные с синтезом кассеты, разрабатываются и выполняются в институте Гамалеи. Затем вакцина, то есть набор индивидуальных ампул для пациента, возвращается к нам, и мы дорабатываем ее до лекарственной формы.
Сколько планируется использовать неоантигенов в нашей вакцине?
Мы планируем использовать от 20 до 35 неоантигенов. Опухоли, особенно те, которые имеют высокую мутационную нагрузку, постоянно претерпевают изменения. Они обладают свойством клональности, то есть в рамках одного узла опухоли могут содержаться участки, немного отличающиеся друг от друга.
Это бывает потому, что в некоторых участках опухоли происходят мутации, появляются два разных клона опухоли. Они находятся в одном узле, но уже отличаются друг от друга. Эти отличия могут быть связаны с тем, как опухоль борется с иммунной системой или с какими-то другими мутациями.
Фото: Константин Михальчевский / РИА Новости
Чтобы покрыть все эти клоны, которые постоянно появляются, нам нужно использовать максимальное количество неоантигенов, 20-35 неоантигенов статистически позволяют этого достичь.
Это помогает предотвратить метастазирование опухоли и преодолеть ее устойчивость к терапии. Например, если мы применяем химиотерапию, основная масса опухоли может уменьшиться, но остаются те клетки, которые устойчивы к этой химиотерапии. И они могут дать рост опухоли и метастазы, что приводит к тяжелой клинической картине
Чтобы преодолеть эту лекарственную устойчивость, мы стараемся обучить иммунную систему узнавать все или почти все клоны опухоли. Чем больше неоантигенов мы используем, тем лучше будет эффект вакцины.
На платформу мРНК, разработанную в институте Гамалеи, можно загрузить столько данных?
Да, можно загрузить до 40 элементов, если говорить упрощенно. Это то количество, которое помещается в кассету мРНК. Но я уже говорил, что не у всех пациентов можно найти столько неоантигенов.
Сейчас мы занимаемся поиском так называемых полууниверсальных маркеров, которые являются уникальными и нестандартными. Эти маркеры можно сравнить с кирпичиками, которые позволят в будущем быстро определять состав персонального препарата для пациента. Конечно, это не будет универсальное решение для всех, но из сотен и тысяч возможных вариантов можно подобрать 20-30 наиболее подходящих для каждого конкретного пациента.
Это направление, в котором мы движемся. Мы не ограничиваемся уже существующими подходами, а продолжаем развивать технологию и надеемся, что в ближайшие годы сможем значительно улучшить ее, даже по сравнению с мировыми аналогами. Но это мы увидим в будущем.
Сколько времени займет процесс изготовления индивидуальной вакцины?
При условии, что все этапы будут выполняться быстро и качественно, — не больше шести-восьми недель. В мировой практике уже есть подобные разработки, и сроки там примерно такие же.
Вакцинация будет применяться соло или в комплексной онкотерапии?
Вакцина может изменить существующие клинические практики, но она не заменит другие методы лечения, а будет дополнять их, особенно в сочетании с другими методами иммунотерапии.
«Наша цель — максимально увеличить безрецидивный период»
Я правильно понимаю, что вакцина — это скорее профилактика рецидива рака?
Совершенно верно, это терапевтическая вакцина, которую применяют после того, как заболевание уже возникло. Мы не можем предсказать, какая опухоль появится у конкретного человека, поэтому не можем предложить ему вакцину, которая предотвратит развитие рака, если его еще нет.
Но когда опухоль уже появилась, мы можем определить ее особенности и исходя из этих генетических характеристик создать вакцину для конкретного пациента. Эта вакцина будет направлена на борьбу с рецидивом, то есть на профилактику повторного развития опухоли. Наша цель — максимально увеличить безрецидивный период
Кроме того, вакцинация поможет в борьбе с метастазами. Когда метастазы уже появились, хирургическое вмешательство может быть затруднено. Однако вакцинация при активной иммунной системе может замедлить или даже уменьшить существующие метастазы.
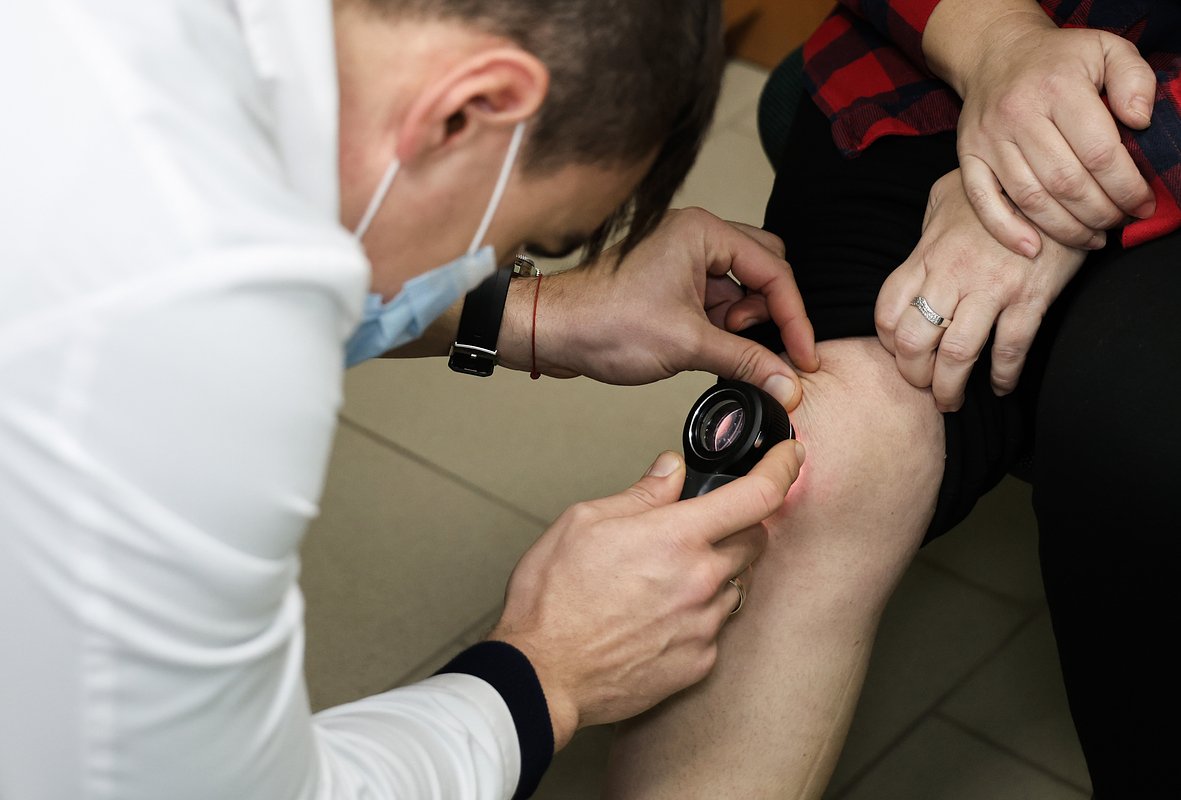
Фото: Сергей Аверин / РИА Новости
Сколько времени онкобольной сможет прожить без рецидива, если он будет использовать вакцину?
Например, в одном из исследований средняя медиана появления рецидива составляла 13 месяцев. У многих пациентов, которые положительно отреагировали на иммунотерапию с использованием вакцины, медиана превысила 24 месяца. И это только наблюдаемый период. Возможно, срок больше. Это говорит о довольно значительном удлинении. Реакция на иммунотерапию с вакциной примерно в два раза сильнее, чем только на иммунотерапию ингибиторами контрольных точек.
И как часто нужно будет вакцинироваться?
Сначала пациент пройдет курс из семи-восьми инъекций с интервалом в несколько недель. После этого мы проверим, появился ли у него иммунный ответ на вакцину. Для этого будут использоваться специальные диагностические подходы, которые помогут определить ее эффективность. В дальнейшем пациент станет получать периодические инъекции этой вакцины до рецидива, возможно — пожизненно. Но пока мы загадываем вперед на три-четыре года, затем нужно будет оценить клиническую практику.
Сколько пациентов, по вашим оценкам, смогут получить пользу от онковакцины?
Не так много, это не миллионы и не десятки тысяч. В масштабах страны, может быть, речь о нескольких тысячах человек, но для них это будет большим шансом на продление жизни.
Вероятно, это будет стоить очень дорого?
Множество клинических технологий стоят сопоставимо или даже дороже. Но они активно используются в клинической практике. Государство наши разработки активно поддерживает.
«Профилактические вакцины маловероятны»
Какие вакцины от рака сегодня существуют в мире и насколько они эффективны?
Противораковые вакцины имеют разные платформы. Это могут быть выделенные белки на специальных носителях, пептидные вакцины, а также неоантигенные вакцины, созданные для каждого пациента индивидуально.
Одним из самых передовых и популярных направлений являются мРНК-вакцины. Также есть разработки, основанные не на персональных антигенах, а на часто встречающихся опухолевых антигенах. Это универсальные вакцины, которые обычно имеют низкую эффективность.
Фото: Евгений Биятов / РИА Новости
Чем хорош персональный подход? Мы обучаем иммунную систему распознавать опухолевые клетки среди множества других клеток, используя 20-30 неоантигенов. Это как если бы мы делали не один выстрел, а двадцать. Большинство ранее разработанных вакцин не показали клинической эффективности в клинических исследованиях. Это связано с тем, что они были универсальными и нацелены на две-три мишени. Однако проблема универсальности в том, что такие антигены малоиммуногенны. Если бы они были иммуногенными, они не были бы универсальными, потому что иммунная система быстро бы их уничтожила. Персонализированные вакцины показали эффективность, значительно превышающую результаты предыдущих подходов.
Каков средний процент эффективности онкологических вакцин?
Для каждого вида рака ситуация может отличаться. Проблема заключается в том, что эффективность лечения может варьироваться в зависимости от различных факторов, таких как тип опухоли, стадия заболевания, состояние пациента и других. В некоторых случаях терапия с использованием контрольных точек может быть эффективна на 10-15 процентов, а в других — на 40 процентов. Однако это лишь общие цифры.
На данный момент можно сказать, что иммунотерапия становится эффективней в среднем в два раза. Это означает, что большее количество пациентов будет положительно реагировать на лечение и демонстрировать хороший клинический ответ. Этот ответ может проявляться в стабилизации заболевания, регрессии опухоли или удлинении периода без рецидивов.
Вы уже говорили о том, что вакцина разработана для лечения, а можно ли создать профилактическую вакцину, о которой все мечтают?
Вряд ли это возможно. Как я уже упоминал в начале, рак — это не одно заболевание, а огромное количество разнообразных болезней с разным происхождением, в разных тканях и с разным течением.
Фото: Гавриил Григоров / ТАСС
Нельзя создать универсальную вакцину сразу от всех вирусов и инфекционных заболеваний. Мы можем разработать вакцину против двух-трех видов инфекций, но их сотни, и невозможно создать вакцину от всех. Точно так же нельзя создать универсальную вакцину от всех видов рака.
Поэтому, к сожалению, профилактические вакцины маловероятны. Но есть и исключения. Например, если мы точно знаем, что причиной определенного вида рака является вирус папилломы человека, как в случае с раком шейки матки, то мы можем создать вакцину против этого вируса. Это не будет вакцина против рака, но она будет направлена против причины его возникновения. Такие вакцины уже существуют и применяются. Они показывают высокую эффективность в снижении риска развития рака шейки матки у женщин.