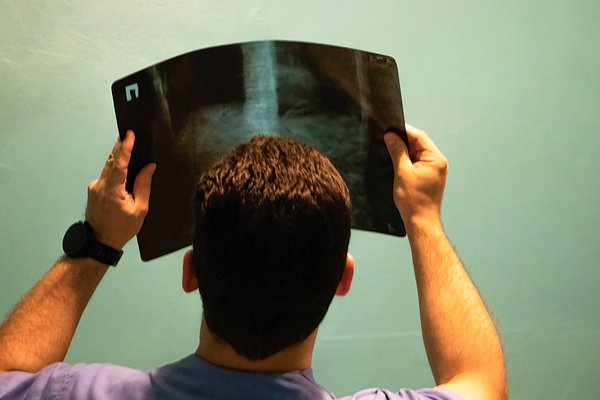
Современная медицина позволяет выявлять рак на самых ранних стадиях. Это способствует снижению смертности — с одной стороны, с другой — часто является причиной гипердиагностики. Ведь если небольшую опухоль обнаружили на скрининге у пациента, которого ничто не беспокоит, значит, нужно что-то делать, даже если человек не нуждается в лечении. А лечение в онкологии создает дополнительный стресс для организма, не говоря об обычном стрессе, который ожидает пациента после постановки диагноза. О том, почему с некоторыми видами рака спешить нельзя и когда скрининг становится бессмысленным, «Лента.ру» поговорила с Максимом Котовым, хирургом НМИЦ онкологии имени Петрова, членом попечительского совета фонда «Не напрасно».
«Лента.ру»: Правда ли, что есть безопасный рак, который не надо лечить?
Максим Котов: Если говорить по-простому, то ответ — нет. Совсем безопасного рака, о котором можно просто забыть, не существует. Все зависит от ситуации.
Действительно, есть опухоли, которые растут годами и никак себя не проявляют. У них высокие показатели выживаемости, и чаще всего их находят случайно — когда человек проходит диспансеризацию или обследуется по другому поводу. Если бы не эти обследования, опухоль никогда бы не нашли и она никак не повлияла бы на продолжительность или качество жизни.
Но мы не можем точно предсказать, как поведет себя та или иная опухоль. Да, на основании исследований мы понимаем, что какой-то тип рака, скорее всего, будет развиваться очень медленно. Но бывают случаи, когда опухоль годами вела себя спокойно, а потом резко начинала прогрессировать.
Предсказать, как будет развиваться рак у конкретного человека, очень сложно: слишком много факторов влияют — и образ жизни, и окружающая среда, и другие заболевания
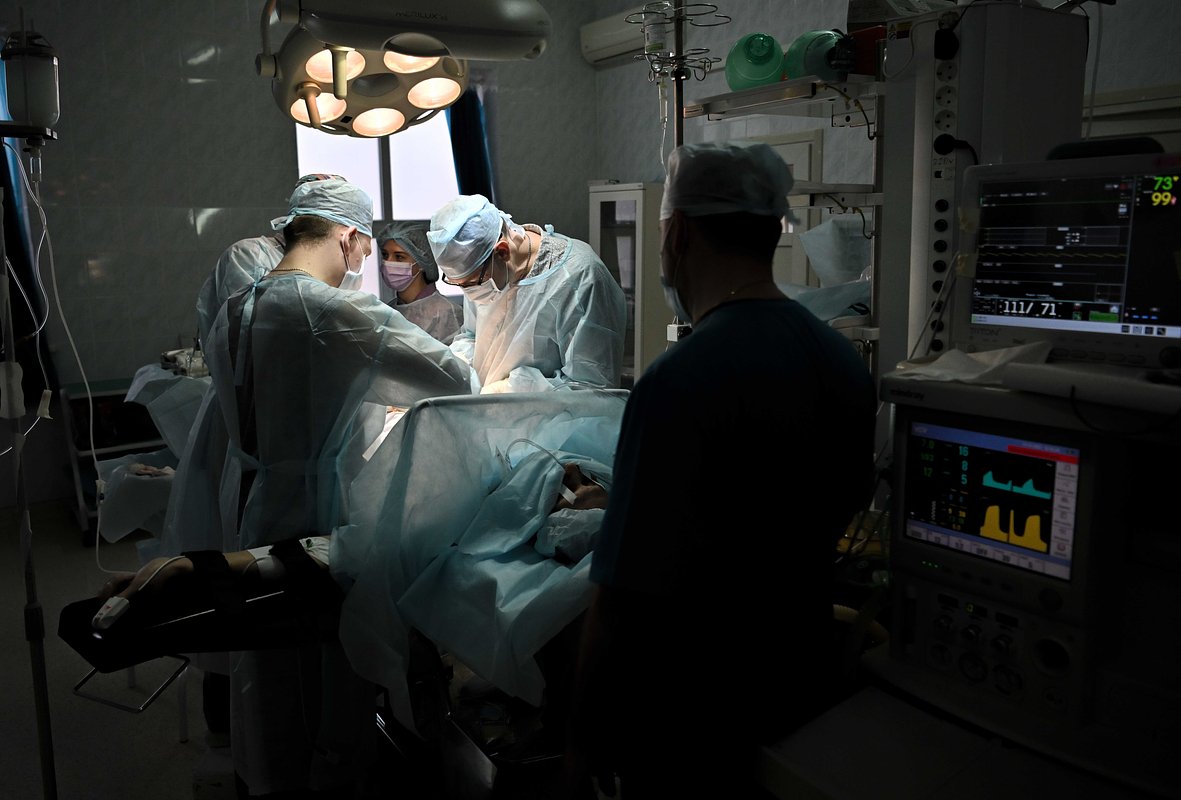
Фото: Евгений Биятов / РИА Новости
Возьмем, например, рак щитовидной железы. Есть так называемые папиллярные микрокарциномы — они маленькие и в целом не растут. Пионеры в этой области — Япония и Корея — накопили огромный опыт наблюдения за такими пациентами. Часть этих людей со временем все равно приходит к хирургическому лечению. Кто-то через год, кто-то через пять лет. Причины разные. Иногда медицинские — если опухоль начала увеличиваться. А иногда чисто психологические: человеку надоело жить с мыслью, что у него рак, надоело постоянно ходить по врачам и обследоваться. И он выбирает операцию, чтобы просто закрыть этот вопрос.
Врачи в таких случаях что обычно советуют?
Мы всегда смотрим на конкретную ситуацию. Ключевой фактор — ожидаемая продолжительность жизни. Если пациент пожилой, у него есть другие болезни, а опухоль маленькая и с низким риском роста, мы понимаем, что он, скорее всего, умрет не от этого рака, а от чего-то другого. И наше вмешательство — операция, химиотерапия — несет гораздо больше рисков, чем сама опухоль. Тогда мы действительно можем предложить активное наблюдение вместо немедленного лечения.
Но если мы обнаруживаем такую же опухоль у молодого человека — баланс между пользой и риском совсем другой. Здесь мы, скорее всего, будем рекомендовать лечение.
Рак щитовидной железы
Классический пример — папиллярная микрокарцинома. Согласно последним международным рекомендациям Американской тиреоидологической ассоциации, обновленным в 2025 году, и Корейской тиреоидологической ассоциации, активное наблюдение считается полноценной альтернативой хирургии. Исследования из Японии и Кореи, которые длились более десяти лет, доказали, что результаты у пациентов, которые просто наблюдали за опухолью, и у тех, кто сразу лег под нож, одинаковые. При этом после операции возможны проблемы с голосом (осиплость) или нарушение работы околощитовидных желез.
Рак предстательной железы
Второй пример — рак простаты низкого риска (Gleason 6). Знаменитое исследование ProtecT — крупнейшее рандомизированное клиническое исследование, которое сравнивало три подхода к лечению локализованного рака предстательной железы: активное наблюдение, радикальную простатэктомию (удаление простаты) и лучевую терапию — наблюдало за пациентами 15 лет и показало, что выживаемость пациентов с этим диагнозом одинаковая. Она составляет 97 процентов независимо от того, выбрал мужчина активное наблюдение, операцию или лучевую терапию. Американские рекомендации NCCN, считающиеся одними из самых авторитетных в мире, советуют активное наблюдение мужчинам с очень низким риском, если им осталось жить меньше двадцати лет, и просто низким — если меньше десяти. Расчеты показывают, что немедленная операция улучшает выживаемость всего на один процент за двадцать лет по сравнению с простым наблюдением.
Рак почки
Небольшие опухоли почки (до четырех сантиметров) все чаще находят случайно, когда человек обследуется по другим поводам. Данные регистра DISSRM говорят о том, что при активном наблюдении выживаемость за пять лет составляет сто процентов, а метастазы появляются только в одном-двух случаях из ста. Кроме того, 20-30 процентов удаленных образований на самом деле оказываются доброкачественными — то есть операция была напрасной.
Хронический лимфолейкоз
Только одному из трех пациентов на момент постановки диагноза действительно требуется лечение. Исследования не обнаружили преимуществ ранней терапии у бессимптомных пациентов.
Фолликулярная лимфома
Ее часто не оперируют и не лечат сразу, потому что она может годами не влиять на продолжительность жизни. А химиотерапия при таком диагнозе — тяжелая и токсичная. Риск осложнений от лечения оказывается выше, чем риски от самой болезни.
***
Здесь перечислены самые известные и распространенные «медленные» виды рака, с которыми врачи сталкиваются постоянно. Во всех этих случаях врачи все чаще выбирают тактику наблюдения — это результат накопленных научных данных. При некоторых типах опухолей стратегия активного наблюдения так же безопасна, как и немедленное лечение.
Вы сказали, что при стратегии наблюдения важно регулярно обследоваться. А если молодой пациент из деревни и у него просто нет возможности часто ездить к врачу?
Это тоже важный фактор, который влияет на решение: где человек живет и насколько ему доступна медицинская помощь. Если у него нет возможности регулярно наблюдаться и при этом лечение не несет запредельных рисков — конечно, мы будем склоняться к операции, чтобы избавиться от опухоли раз и навсегда. Но окончательное решение всегда принимаем вместе с пациентом, обязательно спрашиваем его мнение.

Фото: Кирилл Кухмарь / ТАСС
Рак простаты — один из самых «медленных» видов рака. При нем часто предлагают активное наблюдение вместо операции. Люди соглашаются или боятся, что их недолечивают?
В основном пациенты с диагностированным раком, даже если он низкой степени агрессивности, выбирают радикальное лечение. Это мой опыт. Здесь сильно влияет менталитет: у нас в обществе рак до сих пор воспринимается как приговор. Если рак — значит, надо что-то делать. Срочно.
И не всегда легко донести до человека, что порой лечение бывает хуже, чем его отсутствие. Ведь операция, облучение или химия могут дать такие осложнения, которые серьезно испортят жизнь, а сама опухоль, скорее всего, никогда бы о себе не заявила
Онколог Максим Котов по просьбе «Ленты.ру» составил памятку: кому, когда и как проверяться на рак, чтобы обследования приносили пользу.
Рак молочной железы
- Возраст: с 45 лет (возможно с 40 лет после консультации с врачом)
- Метод: маммография каждые год-два до 74 лет
Рак толстого кишечника
- Возраст: с 45 лет
- Методы: колоноскопия раз в 10 лет (золотой стандарт) или ежегодный иммунохимический тест кала на скрытую кровь
Рак шейки матки
- Метод для 21-29 лет: ПАП-тест раз в три года
- Метод для 30-65 лет: ВПЧ-тест или ко-тестирование (ПАП + ВПЧ) каждые пять лет
- Метод после 65 лет: при стабильно отрицательных результатах предыдущих тестов скрининг можно прекратить
ПАП-тест (цитологическое исследование мазка с шейки матки) позволяет обнаружить атипичные клетки. Жидкостная цитология считается наиболее информативным вариантом. ВПЧ-тест выявляет вирус папилломы человека высокого канцерогенного риска — основную причину рака шейки матки. Ко-тестирование (комбинация двух тестов) обеспечивает максимальную точность.
Рак легких
- Для кого: курильщики и экс-курильщики со стажем от 20 пачко-лет в возрасте 50-80 лет (рассчитать стаж можно по формуле)
- Метод: низкодозная компьютерная томография (НДКТ) ежегодно
Рак предстательной железы
- Возраст: обычно с 45–50 лет после консультации с врачом
- Метод: анализ крови на ПСА. Скрининг требует индивидуального обсуждения с врачом, так как может привести к гипердиагностике и ненужным вмешательствам
Эти рекомендации касаются людей без симптомов и без отягощенной наследственности. При наличии семейной истории рака сроки начала обследований сдвигаются на более ранний возраст. Скрининг обязательно нужно обсуждать с врачом.
Коммерческие чекапы «все включено» с онкомаркерами, ПЭТ-КТ всего тела «на всякий случай» и МРТ всего тела у бессимптомного пациента — это не профилактика, а путь к гипердиагностике и каскаду ненужных обследований. Поэтому онколог рекомендует следующую стратегию.
***
- Знать индивидуальные факторы риска. Семейный анамнез (случаи рака у близких родственников), наследственные синдромы (например, BRCA, синдром Линча), курение, возраст — все это определяет, нужен ли вам более ранний или более частый скрининг. Пройдите бесплатную оценку риска онкологических заболеваний с помощью теста «СКРИН» от фонда «Не напрасно».
- При обнаружении новообразования проходить тщательную диагностику. Найденное образование — не всегда злокачественная опухоль. Большинство из них оказываются доброкачественными или клинически незначимыми (то есть такими, которые никогда не повлияют на здоровье). Прежде чем соглашаться на операцию, рекомендуется получить второе мнение, обсудить с врачом все варианты, включая активное наблюдение, и понять реальный прогноз. Бесплатно это можно сделать с сервисом «Просто спросить» от фонда «Не напрасно».
- Выбрать врача, который говорит о рисках лечения так же честно, как о рисках болезни. Хороший онколог обсудит не только «что будет, если не лечить», но и «что будет, если лечить», отмечает Котов, а именно — побочные эффекты операции, химиотерапии, лучевой терапии. Совместное принятие решений — основа современной онкологии. Если врач говорит только про радикальное лечение, не имея прочных обоснований, и не обсуждает альтернативы — это повод обратиться за вторым мнением.
А если пациент согласился ждать и наблюдать, а потом пошел за вторым мнением, и там ему сказали: «Давайте резать, чего ждать?» Что происходит в такой ситуации?
Из моего опыта, чаще люди все-таки прислушиваются к тому врачу, который предлагает активные действия. Лекарство, операция, вмешательство — это понятно. Знать, что у тебя внутри опухоль, и ничего с ней не надо делать — для нашего менталитета это очень странно и страшно.
Плюс бытовые факторы. Если пациент живет в отдаленном районе, где нет возможности регулярно наблюдаться, делать УЗИ и сдавать анализы, ему проще один раз лечь под нож и решить проблему. Тем более что опухоли, о которых мы говорим, обычно маленькие, и их действительно можно вылечить полностью.
Но если человек готов и может регулярно наблюдаться, мы, конечно, оставляем ему эту возможность. Активное наблюдение — стандартный протокол. Мы не бросаем пациента, а ведем его: смотрим динамику, контролируем размеры, оцениваем риски. И только если опухоль начинает расти или появляются другие тревожные признаки, мы возвращаемся к вопросу об операции. Или если сам пациент говорит: «Все, доктор, я устал бояться, давайте резать». Психологический дискомфорт — тоже уважительная причина.
Сколько обычно проходит времени от обнаружения «медленной» опухоли до того, как она начинает меняться и расти?
Оценить это очень сложно. Исследователи считают, что, например, для щитовидной железы этот период может составлять шесть-семь лет. А может вообще никогда не наступить — опухоль способна никак себя не проявлять.
Проблема в том, что в какой-то момент она все же может начать расти достаточно активно. Но предсказать, когда именно это произойдет, пока невозможно.
Как часто в таком случае нужно обследоваться, чтобы не пропустить этот момент?
Обычно рекомендуют проходить контроль раз в полгода.
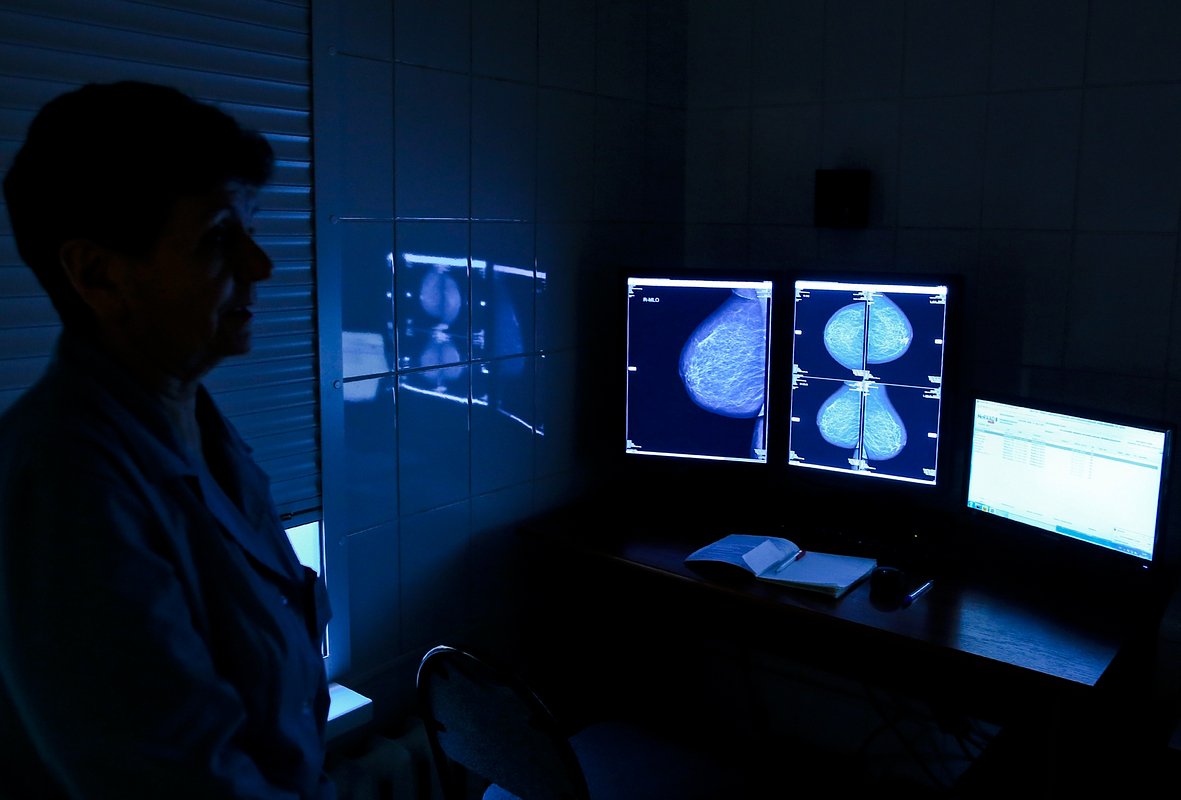
Фото: Максим Змеев / PhotoXPress
Маммографию называют золотым стандартом скрининга рака молочной железы. Но сейчас появляются исследования, которые показывают, что за десять лет каждая вторая женщина хотя бы раз сталкивается с ложным подозрением на рак. Мы точно не переоцениваем пользу маммографии? Может, от нее больше вреда?
Скрининг — это вообще очень интересная история. Его польза всегда считается не для конкретного человека, а для популяции в целом. Все программы разрабатывались с учетом населения — города, страны и так далее.
Цель любого скрининга — снизить смертность от рака. И если он эту задачу выполняет — значит, метод работает. Но здесь важно понимать статистику. Например, чтобы спасти одну жизнь от рака молочной железы, нужно сделать несколько тысяч маммографий. То есть цифры очень большие. Количество раков, которые мы выявляем при скрининге, на самом деле невелико. А количество тех, которые мы успели поймать на ранней стадии и действительно предотвратили смерть, — еще меньше.
Получается парадокс. Для популяции в целом скрининг работает, смертность снижается. Но для конкретных женщин польза уже не так очевидна
С одной стороны, мы действительно можем обнаружить опухоль на ранней стадии и спасти жизнь. С другой — есть проблема гипердиагностики. Мы можем найти то, что вообще не является раком, но по данным обследования будет выглядеть как рак. И тогда начинается каскад: инвазивная диагностика, биопсии, а иногда и операции. А это уже реальные риски: инфекции, кровотечения, осложнения. Плюс психологический фактор: тревога, стресс, жизнь в неопределенности.
И есть еще такое понятие, как интервальные раки. Представьте: женщина прошла маммографию, все хорошо. А через год приходит на следующую — и там уже опухоль, которая выросла и развилась как раз в промежутке между обследованиями.
Поэтому ответ не может быть однозначным. Маммография — работающий инструмент, но со своими ограничениями и рисками.

Фото: Алексей Сухоруков / РИА Новости
Так делать или нет? Скрининг в итоге нужен?
Глобально — делать. Потому что у нас есть данные: скрининг действительно снижает смертность от рака. Но важно понимать, что это работает только для определенных типов опухолей.
Скрининг доказанно эффективен для рака молочной железы, шейки матки, рака толстого кишечника, рака легкого (в группах риска) и рака предстательной железы. Для всех остальных типов опухолей, а их больше трехсот разновидностей, польза массового скрининга — под большим вопросом. Там работает уже не скрининг, а ранняя диагностика. И это принципиально разные вещи.
Скрининг — когда человек чувствует себя здоровым, ничто не беспокоит, но есть факторы риска, прежде всего — возраст. Мы предлагаем ему провериться. Ранняя диагностика — это когда симптом уже есть. Например, появилась родинка, которая изменилась. Человек идет к врачу, тот смотрит, делает дерматоскопию и решает, что делать. Наличие родинки — уже симптом, повод для визита, но это не скрининг, а диагностика возникшей проблемы.
Мы часто говорим о пользе раннего выявления, но редко — о вреде самой диагностики. Например, биопсия простаты чревата инфекциями, вплоть до сепсиса. Как вы для себя оцениваете это соотношение: когда риск оправдан, а когда нет?
У скрининга, как и у любой медицинской процедуры, есть плюсы и минусы. Плюс очевидный — раннее выявление рака, которое повышает шансы на эффективное лечение и снижает риск смерти. Минусы — гипердиагностика и связанные с ней инвазивные процедуры, у которых есть свои осложнения.
При трансректальной биопсии предстательной железы риск инфекционных осложнений составляет от 0,5 до 9,4 процента для сепсиса, для инфекций мочевыводящих путей с лихорадкой — от 0,3 до 4,9 процента. Это не абстрактные проценты, а реальные риски. Для сравнения: при колоноскопии риск перфорации кишечника — одна на десять тысяч исследований. Тоже редкое, но серьезное осложнение.

Фото: Ростислав Нетисов / РИА Новости
Поэтому решение о биопсии всегда проходит через фильтр «риск — польза». Мы смотрим на возраст пациента, на другие его заболевания. И главное — задаем себе вопрос: если мы найдем рак, сможет ли этот человек перенести специализированное лечение — хирургию, лучевую или химиотерапию?
Если мы подозреваем опухоль, которая может расти и метастазировать, и без лечения она убьет пациента, биопсия необходима. Без нее мы не можем определить тип опухоли и назначить правильное лечение
Но здесь крайне важна коммуникация с пациентом. Надо объяснять все варианты, все плюсы и минусы — и не только с медицинской точки зрения, но и с точки зрения его жизни. Пациент должен понимать, во что он ввязывается, чтобы участвовать в принятии решений. А наша задача — максимально обезопасить это решение.
Вы говорили, что для возрастных пациентов часто выбирают не лечение, а наблюдение. А с какого возраста регулярные скрининги можно уже не проходить?
В большинстве случаев скрининг прекращают в 70-75 лет. Если мы что-то обнаружим в этом возрасте, выигрыш для пациента будет уже очень маленьким. Чем старше человек, тем выше риски умереть от других причин — сердечно-сосудистых заболеваний, возрастных изменений.
Все скрининговые программы — маммография, колоноскопия, анализ на скрытую кровь — основаны на научных исследованиях. И они показали: после определенного возраста преимущества скрининга исчезают. То есть нет разницы в смертности между теми, кто продолжает проверяться, и теми, кто уже не проверяется.
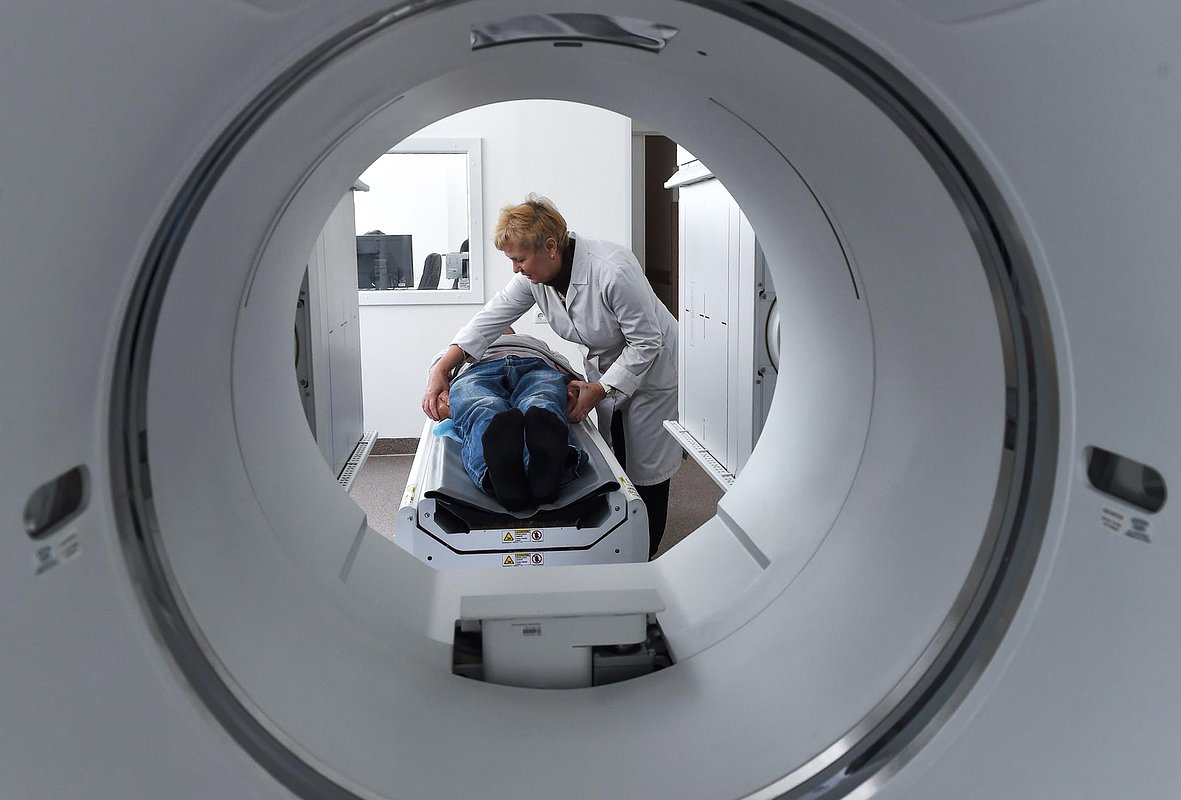
Фото: Виктор Коротаев / Коммерсантъ
То есть если родственники привели пожилую бабушку в больницу и настаивают на полном чекапе, а у нее ничего не болит, врач должен отказать?
Если ничего не беспокоит, по большому счету смысла в тотальной проверке действительно нет. Другое дело, что многие процедуры сами по себе не опасны — например, маммография дает небольшую лучевую нагрузку. Но вопрос не в том, можно ли сделать тест. Вопрос в том, что мы будем делать с результатом. Мы что-то найдем — и дальше что? Если мы не готовы лечить или лечение принесет больше вреда, чем пользы, то зачем мы это делали?
Просто делать тест ради теста смысла нет
Одна из главных проблем сегодня — невозможность точно предсказать, как поведет себя опухоль, насколько она агрессивна. А есть тесты или исследования, которые могут это сделать?
Исследования в этом направлении ведутся. Речь идет о том, чтобы предсказывать активность опухоли, скорость ее роста и распространения. Но проблема в том, что такие тесты существуют далеко не для всех видов рака.
Сейчас лучше всего это работает для рака молочной и предстательной железы. Мы можем посмотреть на определенные мутации, гены, проанализировать большие массивы данных и на основе этого сделать прогноз в процентах.


Но для многих других опухолей таких маркеров просто нет. У них нет той генетической вариабельности, нет биохимического или генетического маркера, который можно было бы использовать для создания подобных тестов. Тем не менее направление перспективное. Эти тесты нужны, чтобы более индивидуально подходить к выбору лечения: лечить или не лечить, какую интенсивность лечения выбрать.
Вот пример из онкологии. Есть понятие «адъювантная терапия» — лечение после радикальной операции, химиотерапия или иммунотерапия при раке, например, молочной железы. Исследования показывают, что адъювантная терапия снижает риск рецидива. Но далеко не всем пациентам это снижение реально нужно.
Если мы, например, пролечим тысячу человек, только один получит реальную пользу. Остальные 999 перенесут токсичную химиотерапию с побочными эффектами, но никакого выигрыша в выживаемости не получат
Та же логика работает и в скрининге. Мы можем сделать маммографию десяти тысячам женщин, найти несколько ранних раков, спасти пару жизней — а остальные пройдут через ложную тревогу и ненужные биопсии.
Поэтому задача молекулярных и генетических тестов — сделать скрининг более точным и индивидуальным. Чтобы он работал не просто на уровне популяции, где польза доказана статистически, а на уровне конкретного человека. Чтобы мы понимали, что этому человеку скрининг действительно нужен, а этому — не обязателен. Это и есть медицина будущего: отказ от подхода «лечить всех подряд» в пользу точного, персонализированного выбора.