В четверг, 20 мая, в журнале Science появилась очень необычная работа. В ней сообщалось, что группе исследователей удалось создать организм с синтетическим геномом. Ученые получили обыкновенную на вид бактерию, которая ничем не отличалась от других бактерий за исключением одного: ее ДНК - молекула, определяющая все свойства клетки, - была от первой и до последней "буквы" синтезирована искусственно.
Представьте: обычный дождливый октябрьский вечер 2158 года. Житель, скажем, Северного Чертанова возвращается к себе и домой и решает, что топливо в его машине ему окончательно разонравилось. Он подходит к компьютеру и пишет заявку в компанию, чтобы ему прислали новых бактерий, которые вырабатывают более качественное горючее. Написанное кажется полным бредом, однако не исключено, что такое или почти такое будущее человечеству открывает новая работа, появившаяся в журнале Science.
Работа называется "Создание бактериальной клетки, которая контролируется химически синтезированным геномом". Схема проведенного учеными эксперимента очень проста: они взяли несколько банок реактивов, синтезировали из них геном бактерии и вставили его в клетку другой бактерии, из которой заранее удалили собственную ДНК. На реализацию этой несложной схемы на практике у исследователей ушел не один год.
Читатель может спросить, а зачем вообще ученые взялись за такую странную задачу - синтезировать de novo то, что и так уже создано природой? Ответ на этот вопрос очень прост: потому что этой работой руководил Крейг Вентер (Craig Venter). Это имя хорошо известно тем, кто связан с биологией или когда-то интересовался проектом "Геном человека".
Яркая личность
Крейг Вентер занялся наукой после службы в армии и возвращения из Вьетнама. Молодого ветерана интересовала биохимия, и именно в этой области он получил сначала степень бакалавра, а потом доктора философии (с некоторыми оговорками - аналог нашей степени кандидата наук, в данном случае биологических). Вентер не был "классическим" ученым, который не вылезает из своей лаборатории и всячески избегает любой административной и коммерческой деятельности. В 1998 году будущий создатель искусственного генома принял участие в организации биотехнологической компании Celera Genomics.
Именно в Celera Genomics была впервые определена полная геномная последовательность живого организма - дебютантом стал микроорганизм Haemophilus influenzae. Компания занялась расшифровкой бактериальных геномов не просто так - в 1990 году был запущен глобальный проект по определению последовательности ДНК Homo sapiens "Геном человека". На момент создания Celera Genomics сотни ученых из разных стран мира не смогли полностью расшифровать последовательность ни одной из 23 пар хромосом человека. В 1999 году была "сделана" самая маленькая (как считалось тогда) 23-я хромосома. Причиной столь медленного прогресса являлось несовершенство технологий секвенирования (определения последовательности) ДНК.

Крейг Вентер изучает образцы, собранные во время морской экспедиции. Фото с сайта jcvi.org
Lenta.ru
Вентер разработал новый подход к секвенированию, названный методом "дробовика" (shotgun sequencing), который оказался намного эффективнее традиционных методов. В 2000 году благодаря "дробовику" была завершена черновая расшифровка генома человека. Однако генетические данные не были выложены в общий доступ, как это принято в научной среде, - Вентер изначально планировал продавать расшифрованные им последовательности. Меркантильный подход к столь важной для человечества проблеме вызвал у ученых негодование, и в конце концов Вентер был вынужден открыть полученную им информацию.
Сразу после завершения проекта "Геном человека" Вентер ушел из Celera Genomics по не до конца ясным причинам (ходят более чем упорные слухи, что Вентер покинул компанию из-за конфликта с руководством) и основал институт имени себя. Параллельно он организовал морскую экспедицию на корабле Sorcerer II, в ходе которой обнаружил тысячи новых видов живых существ.
Основными проектами Крейга Вентера и его института стали создание организма с минимальным геномом и организма, геном которого будет создан учеными искусственно. Первое направление подразумевает получение жизнеспособного существа, в геноме которого присутствуют только самые необходимые гены. Иными словами, удаление любого из них неминуемо должно приводить к гибели такого генетического "спартанца". Этот проект пока находится в стадии разработки. А вот второе направление - по созданию существа с химически синтезированным геномом - завершилось успехом.
Дело техники
Для того чтобы отличать "неестественную" ДНК от "естественной", ученые не точно воссоздавали геном M. mycoides: в некоторые регионы, которые не кодируют гены, они вставляли специальные "флажки", представляющие собой короткие фрагменты ДНК определенной последовательности. Предварительно исследователи убедились, что вставка "флажков" не влияет на жизнеспособность бактерий.
На роль первого искусственного существа, как многие СМИ уже окрестили продукт экспериментов Вентера, была выбрана паразитическая бактерия Mycoplasma mycoides. Микроорганизмы из рода Mycoplasma являются излюбленными модельными организмами Вентера из-за своего генома - он у них очень маленький. ДНК M. mycoides состоит всего лишь из миллиона нуклеотидов - элементарных "кирпичиков", а, например, ДНК человека включает три миллиарда нуклеотидов. Раньше исследователи из института имени Крейга Вентера работали с бактериями M. genitalium, однако они очень медленно растут, и ученые переключились на более "расторопных" M. mycoides.
Первой частью работы стало определение последовательности генома M. mycoides. Хотя еще десять лет назад молекулярные биологи выбивались из сил, пытаясь "прочитать" человеческие хромосомы, сейчас секвенирование стало совершенно рутинной операцией, не требующей особых усилий. Правда, для создания организма с синтетическим геномом исследователи расшифровывали ДНК намного более тщательно, чем обычно. То есть они определили полную геномную последовательность M. mycoides не один или два раза, а как минимум десять. Такие повторные эксперименты позволяют обнаружить и исправить ошибки, неизбежно присутствующие при однократном "прочтении".
На следующей стадии эксперимента Вентер и его коллеги, используя полученную и выверенную последовательность ДНК M. mycoides как образец, начали химически синтезировать геном этой бактерии из отдельных нуклеотидов, созданных промышленным способом - в буквальном смысле на фабрике. Но несмотря на колоссальную скорость развития молекулярно-биологических технологий синтезировать за раз очень длинные последовательности ученые пока не умеют: когда цепь ДНК дорастает до нескольких сотен тысяч нуклеотидов, она начинает путаться и рваться. По этой причине исследователи синтезировали целый геном M. mycoides по кусочкам – авторы назвали их кассетами - длиной около тысячи нуклеотидов, а потом собирали геномный паззл воедино.
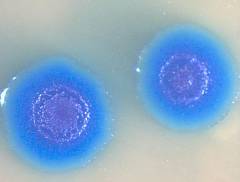
Колонии Mycoplasma mycoides, полученные при помощи вставки искусственного генома в клетки M. capricolum. Фото авторов исследования
Lenta.ru
В качестве устройств для сборки кассет ученые использовали живые клетки – их ферментативные системы "склеивают" фрагменты ДНК с такой точностью, которой невозможно добиться при химическом соединении. "Склейку" проводили в три этапа: сначала ученые совмещали кассеты по тысяче нуклеотидов и получали фрагменты длиной в 10 тысяч "букв". Потом эти "заготовки" соединяли друг с другом, чтобы получить фрагменты в 100 тысяч нуклеотидов, которые, наконец, объединяли в целый геном. Все эти операции проводили сначала в клетках кишечной палочки, потом, когда генетический полуфабрикат дорос до сотен тысяч нуклеотидов, в клетках дрожжей.
На последней стадии эксперимента ученые поместили созданный ими геном M. mycoides в лишенные ДНК клетки "родственных" бактерий M. capricolum. Так как все свойства живых существ, в том числе и видовая принадлежность, определяются их ДНК, после вставки в клетку M. capricolum генома M. mycoides "на выходе" должны были получиться… правильно, M. mycoides. Именно так и вышло: "гибриды" выглядели как настоящие M. mycoides, с той же скоростью поглощали питательные вещества, росли теми же темпами и даже состав их белков практически не отличался от белков M. mycoides, появившихся на свет обычным способом.
Если бы ученые помещали химически синтезированный геном в клетку бактерии того же вида, результаты эксперимента нельзя было бы трактовать однозначно. Например, можно было бы заявить, что сходство "гибридов" с M. mycoides определяется не только ДНК, но и, например, регуляторными белками, оставшимися в клетках "обычных" M. mycoides.
Зачем?
В своей статье Крейг Вентер пишет, что полученные им и его сотрудниками результаты, во-первых, важны как наглядное доказательство того, что ДНК содержит исчерпывающую информацию об организме, а во-вторых, умение создавать организмы, генетическая программа которых от начала и до конца прописана человеком, сулит, по мнению Вентера, очень заманчивые перспективы практического применения. Например, ученый планирует создать водоросли, которые могли бы синтезировать не только питательные вещества, необходимые им самим, но также множество полезных для человека соединений. Кроме того, Вентер видит у своей технологии большое фармацевтическое будущее: бактерии с синтетическим геномом могут в промышленных масштабах производить новые лекарства.
Однако энтузиазм ученого разделяют далеко не все его коллеги. Например, биолог Евгений Нудлер, профессор биохимии Нью-Йоркского университета и заведующий московской лабораторией молекулярных механизмов старения "Геронлаб", считает, что прямого практического приложения в обозримом будущем эта работа не имеет. "Чудесные организмы, о которых говорит Вентер, можно получить и более простыми способами, которые доступны в любой лаборатории. Сегодня мы умеем изменять гены, всячески тасовать их, вставлять и убирать из генома огромные куски. Для того чтобы сделать, например, бактерию-производителя лекарств, совершенно не обязательно заново создавать целый геном", - рассказал Нудлер "Ленте.Ру". Он также отметил, что технология Вентера неоправданно сложна: "Чем больше фрагмент ДНК, который вы вставляете в геном, тем сложнее его "запихнуть" в клетку. Поэтому намного проще добавить в бактерию только несколько важных вам генов, чем пытаться вставить в нее целый новый геном".
Что касается создания при помощи "генетического программирования" водорослей и других организмов, у которых есть ядро (бактериальная ДНК ничем не отгорожена от остального содержимого клетки), то это, по мнению Нудлера, пока остается столь же недостижимой задачей, как и раньше. "ДНК эукариот (так называют организмы, имеющие ядро, к которым относятся все растения, животные и в том числе человек) устроена намного сложнее, чем бактериальная ДНК. Разработанная Вентером технология просто не будет работать для этих организмов", - объяснил он.
Похожее мнение высказал и биолог Константин Северинов, профессор и заведующий лабораторией в университете Ратгерса, а также лабораториями в институте молекулярной генетики и институте биологии гена: "Для того чтобы повторить этот эксперимент для организмов, клетки которых имеют ядро, потребуется, во-первых, создать "работающие" искусственные хромосомы - в отличие от бактерий, у эукариот с ДНК связано гораздо больше различных белков и большое количество информации имеет эпигенетический характер, то есть не закодировано в самой последовательности ДНК, а, во-вторых, придумать метод помещения ДНК в ядро, из которого удалены предсуществующие хромосомы. Пока у ученых нет технологий, которые позволяют это делать. В качестве альтернативы можно пытаться создавать искусственное ядро, а это исключительно сложная задача".
И тем не менее, Северинов видит в работе Вентера определенный практический смысл: "На сегодня у нас секвенированы геномы тысяч различных живых существ, однако эффективно работать (то есть направленно изменять гены) ученые могут, на самом деле, только с несколькими модельными организмами - кишечной палочкой и небольшим числом других бактерий, дрожжами, червяком-нематодой, лягушкой, мухой и мышью. Используя предложенный Вентером подход, можно было бы брать химически синтезированные мутационные варианты генома неизученных микроорганизмов, помещать их в клетку-реципиент и исследовать свойства таких вариантов. Впрочем, это потребует очень значительного удешевления существующей технологии. А собственно к написанию генетических программ и созданию действительно новых организмов работа Вентера отношения не имеет. Пока он всего лишь реализовал уже существующую в природе программу".
Несмотря на то что однозначного признания результатов Вентера в научном сообществе нет и многие исследователи относятся к ним скептически, работой по созданию синтетического генома уже заинтересовались на самом высшем государственном уровне. Барак Обама распорядился создать специальную комиссию по изучению этического аспекта создания живых клеток при помощи искусственно созданной ДНК. Так что не исключено, что в обозримом будущем дискуссии о работе Вентера перетекут из чисто практической плоскости в философскую.