Все дело в волшебных пузырьках Нобелевскую премию по медицине вручили за везикулярный транспорт
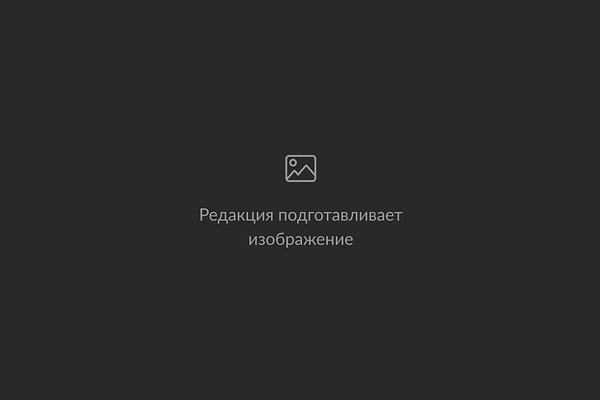
Слияние везикулы с клеточной мембраной: «колбасками» показаны белки-рецепторы SNARE (справа) и вирусные белки, имитирующие их работу (слева). Изображение: Weber et al. 1998
Нобелевскую премию по физиологии и медицине в этом году получили три американских ученых за «исследование механизмов, регулирующих везикулярный транспорт». Ренди Шекман, Джеймс Ротман и Томас Зюдоф в своих работах объяснили, как различные вещества двигаются внутри клеток в мембранных пузырьках: работа каких генов для этого необходима, как на молекулярном уровне происходит слияние везикул и как этот процесс регулируется в нейронах, где особенно важно, чтобы слияние происходило только в нужное время и в нужном месте.
Эукариотическая, то есть содержащая ядро клетка, с точки зрения биохимии, очень велика. Хотя рассмотреть ее обычно можно только в микроскоп (яйца и волокна апельсинов — не в счет), даже самая маленькая эукариотическая клетка больше клетки бактерий в сотни и тысячи раз. Как бы ни была сложна бактерия, она, в конечном счете, не далеко ушла от пробирки с (очень сложным) раствором, но клетки эукариот от безъядерных микробов в этом смысле очень сильно отличаются. Они всегда поделены на множество отделов, которые выполняют разные функции и часто содержат совершенно непохожие, несовместимые вещества.
Это означает, что перед эукариотами, в отличие от бактерий, в какой-то момент эволюции появилась проблема внутриклеточной логистики. До того, как возникли ядерные организмы, такой проблемы не существовало: то, что синтезировалось в одной части бактериальной клетки, немедленно диффундировало в другую ее часть. Если же какое-либо вещество требовалось выбросить в окружающую среду, его обычно синтезировали на мембране, одновременно протаскивая наружу как нитку через игольное ушко.
Однако для большой и сложной клетки эукариот, даже если она представляет собой совершенно самостоятельный организм, без системы внутриклеточного транспорта обойтись нельзя. И уж тем более такая система необходима многоклеточным, некоторые клетки которых специализируются на выработке разных веществ: гормонов, пищеварительных ферментов или нейромедиаторов. Именно поэтому у эукариот, наряду с ядром и митохондриями, появилась другая принципиальная инновация — развитая система транспорта веществ в мембранных пузырьках.
Ренди Шекман: От пузырьков к генам
Следует сразу оговориться, что нынешняя Нобелевская премия присуждена не за открытие везикулярного транспорта как такового, а за выяснение механизма его работы. То, что некоторые вещества могут транспортироваться внутри клеток в пузырьках-контейнерах, стало ясно практически тогда же, когда получил распространение электронный микроскоп — такие пузырьки были ясно видны на снимках. Один из «логистических узлов», где они формируются, аппарат Гольджи, был открыт итальянским ученым Камилло Гольджи еще в конце XIX века, даже до изобретения электронного микроскопа. Второй главный «клеточный хаб», эндоплазматический ретикулум (ЭПР), был открыт несколько позже Альбертом Клодом, за что ученый наряду с двумя коллегами получил Нобелевскую премию по физиологии и медицине в 1974 году. И, наконец, тот факт, что именно мембранные пузырьки с нейромедиаторами передают сигналы от одного нейрона к другому в синапсах, был установлен Катцем, фон Эйлером и Аксельродом, благодаря чему они также стали нобелевскими лауреатами в 1970 году.

Ренди Шекман
Фото: Uwe Dettmar / GBM / AFP
Научным руководителем Шекмана в университете стал Артур Корнберг, нобелевский лауреат и знаменитый биохимик (а также отец нобелевского лауреата Роджера Корнберга, который сейчас вместе с Жоресом Алферовым возглавляет научный совет Сколково).
Несмотря на биохимическую школу, для того чтобы разобраться с везикулярным транспортом, Шекман обратился не к биохимическому, а к генетическому методу исследования. Он решил использовать наиболее простой эукариотический модельный организм, и занялся получением мутантов дрожжей, у которых проявляются те или иные дефекты везикулярного транспорта.
В серии работ, выполненных совместно с Петером Новиком (именно он значится первым автором ключевых статей Шекмана), ученый обнаружил у дрожжей 23 гена, работа которых необходима для нормальной секреции гликопротеинов. Когда мутантные дрожжи переносили в термостат с высокой температурой (там мутации начинали проявлять свое действие), клетки переставали делиться. Под электронным микроскопом по краям таких клеток можно было заметить тысячи маленьких пузырьков, которые не могли слиться с мембраной и выбросить наружу свое содержимое. Испорченные у этих мутантов гены получили названия sec1, sec2, sec3 и так далее. Они стали своего рода библиотекой, на которую ориентировались последующие ученые, когда родственные гены начали искать у высших эукариот. Однако как на молекулярном уровне работают белки, кодирующиеся этими генами, выяснить удалось уже не Шекману, а его независимо работавшему коллеге, Джеймсу Ротману.
Джеймс Ротман: Белковая молния
У Джеймса Ротмана, который всего на два года младше Шекмана и примерно в то же время работал над внутриклеточным транспортом в Стенфорде, был принципиально иной подход к исследованиям. Во-первых, он работал не на дрожжах, а на культурах клеток млекопитающих. Точнее говоря, даже не на самих клетках, а на их экстрактах. Во-вторых, он занимался не поиском мутантов, а классической биохимической работой — выделением белков. В каком-то смысле можно сказать, что Ротман стал «копать тоннель с другого конца» и, к счастью, в 1992 году эти два направления исследований сошлись в одной совместной работе.
box#1427496
Главной моделью Ротмана стал вирус везикулярного стоматита (VSV), один из белков которого при созревании гликозилируется, то есть модифицируется различными сахарами. По мере того как этот белок после синтеза на мембране ЭПР двигается вдоль транспортного «конвейера» клетки, он сначала получает, а потом теряет некоторые сахара. Эти сахара оказались для Ротмана очень удобными маркерами, благодаря которым можно было отследить, на какой стадии остановился транспорт при добавлении тех или иных клеточных экстрактов.
Работая с этой биохимической системой, Ротман выделил сначала один (NSF), а затем множество белков, работа которых была необходима для слияния и деления мембранных пузырьков. И в этот момент работы Шекмана и Ротмана, генетический и биохимический подход, сошлись: оказалось, что один из белков, выделенных из экстрактов клеток (SNAP), является близким родственником того, чья последовательность закодирована геном sec17 из дрожжей. Открытие было опубликовано в первой совместной работе нынешних нобелевских лауреатов, которые до этого момента работали совершенно независимо друг от друга. Помимо прочего, из этого совпадения следовало, что система везикулярного транспорта у дрожжей и млекопитающих работает благодаря одним и тем же общим механизмам.
Дальнейшие биохимические опыты Ротмана позволили установить состав целого комплекса белков, которые участвуют в слиянии молекулярных пузырьков. Для поиска этих молекул ученый использовал уже не экстракты клеточных культур (материала в них обычно довольно мало), а препараты бычьих мозгов, ведь именно в нервной ткани очень много синапсов, где везикулы с нейромедиаторами должны сливаться по команде электрического возбуждения.
Работы Ротмана позволили сформировать так называемую SNARE-гипотезу — модель, которая объясняет, почему везикулы сливаются с клеточными мембранами именно в тех местах, где это необходимо. Согласно этой модели, слияние регулируется двумя группами рецепторов: t-(target)-SNARE (синтаксины) и v-(vesicle)-SNARE (синаптобревины), то есть молекулами, находящимися на мембране и на везикулах соответственно. Определенные рецепторы v-SNARE способны взаимодействовать с рецепторами t-SNARE только строго соответствующего типа (а их известно не менее 35 разновидностей), поэтому слияние проходит специфически, хотя его механизм в общих чертах остается тем же самым.
Ключевым моментом слияния является переплетение находящихся на разных мембранах белков в своеобразные косы из четырех альфа-спиралей (в англоязычной литературе их принято называть «застежками-молниями»). Это переплетение дает энергию, необходимую для слияния липидных слоев, которые в норме достаточно сильно отталкиваются друг от друга из-за отрицательного заряда фосфатов.
Томас Зюдоф: Кальциевая регуляция
После того как молекулярный механизм слияния мембранных пузырьков был выяснен, остался вопрос временнóй регуляции этого процесса. Ведь в нервных клетках везикулы с нейромедиатором должны выбрасываться в синаптическую щель тогда и только тогда, когда клетка возбуждается. Электрическая деполяризация нейрона всегда сопровождает вход в клетки ионов кальция и именно они оказались ключевыми для всего процесса.

Томас Зюдоф
Фото: vanderbilt.edu
Работая на так называемых нокаутных мышах — животных, у которых искусственно выключен один из генов, Зюдоф показал, что удаление комплексина приводит к сильному снижению активности всех без исключения синапсов. Непосредственно связывание ионов кальция проводит другой белок, синаптотагмин. Кроме того, Зюдофом с коллегами был найден и третий белок, который соответствовал тому самому мутанту sec-1, который первым попался Шекману в его исследованиях в конце 70-х.

SNARE комплекс формируется в результате сплетения четырех альфа-спиралей белков синаптобревина (v-SNARE), синтаксина (t-SNARE) и SNAP-25. Синаптотагмин служит кальциевым сенсором.
Изображение: Danko Dimchev Georgiev, M.D.
Интересно, что в ходе этих опытов Зюдофу удалось даже получить линию нокаутных мышей, у которых из-за отсутствия одного из белков во всей нервной системе не работал ни один (!) синапс. Самым удивительным было то, что у таких грызунов формировался практически нормальный мозг, нейроны которого все-таки умирают, но очень поздно — только после его полного созревания. Таким образом, попутно с прояснением деталей регуляции везикулярного транспорта удалось установить, что работа синапсов нужна мозгу для того, чтобы поддерживать свое существование, но не требуется, пока он еще не созрел.
О моде на науку
Прошлогодняя Нобелевская премия по медицине Джону Гардону и Синья Яманаке была вручена за открытие механизма перепрограммирования, который позволяет практически из любых зрелых клеток получить стволовые. Работы двух этих ученых оказались сильно разнесены во времени — ключевые опыты Гардон провел в 70-х годах, а Яманака получил первые перепрограммированные стволовые клетки в 2004 году. Сказать, что этого последнего открытия очень ждали, значит ничего не сказать: оно позволило, наконец, работать со стволовыми клетками без использования эмбрионов и, что еще более важно, научило биологов получать стволовые клетки, которые генетически идентичны донорам материала. Сегодня такие клетки уже вовсю используются для получения искусственных органов. Из них, как недавно показали ученые, даже формируются напоминающие мозг органоиды, а произведенные in situ, такие клетки обладают полной тотипотентностью — они способны даже образовывать внутри тела эмбрионы.

Выделение нейромедиатора из пресинаптической щели, 3D-рендер.
Нобелевский комитет, как мы видим, далеко не всегда следует моде. И это хорошо: на длинной дистанции ценность открытия определяется не его немедленной применимостью, а фундаментальностью, то есть тем, насколько глубинные процессы оно может объяснить.
Если же кому-то очень хочется придать нынешней премии модный флер, то сделать это проще простого. Помните такую косметическую процедуру, как «ботокс», инъекцию ботулотоксина? Так вот, ботулотоксин разрезает как раз те самые открытые Ротманом белки (а именно SNAP-25) в комплексе SNARE-рецепторов в месте слияния везикул, что приводит к выключению данного синапса.