Экспериментальное лекарство восстановило синапсы мозга у мышей с нейродегенерацией, аналогичной той, что наблюдается при болезни Альцгеймера у людей. Результаты исследования, проведенного учеными из Йельского университета, опубликованы в журнале Science Translational Medicine (STM).
Известно, что основной причиной клинического прогрессирования болезни Альцгеймера, начиная от легких когнитивных нарушений и заканчивая тяжелой деменцией, является потеря синапсов — связей между нейронами. При этом важную роль играет связывание бета-амилоидных пептидов Aβo, которые начинают накапливаться в нервных тканях задолго до появления первых симптомов, с клеточным прионным белком PRPC. В предыдущих исследованиях было показано, что Aβo и PRPC влияют на передачу биохимических сигналов внутри нервных клеток через нейрональный метаботропный глутаматный рецептор 5 (mGluR5).
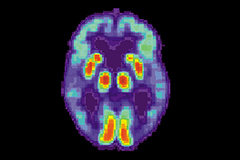
В новой работе ученые использовали аллостерический регулятор BMS-984923, который не блокирует важную для нормального функционирования нейронов передачу сигналов, но ингибирует взаимодействие между прионным белком и mGluR5. Препарат перорально вводили в организм ГМ-мышей, у которых в возрасте 12 месяцев наблюдалась значительная потеря синапсов из-за активности внедренной в геном ДНК человеческого тау-белка и бета-амилоида. Плотность синапсов в мозге оценивали с помощью позитронно-эмиссионной томографии (ПЭТ). BMS-984923 в дозах, безопасных для грызунов и приматов, смог предотвратить негативное влияние бета-амилоидных пептидов на передачу сигналов, связанных с функционированием синапсов. ПЭТ показала, что при этом синаптическая плотность в мозге полностью восстанавливалась. Терапевтический эффект сохранялся даже после вымывания препарата. Ученые также показали, что изменения в глутаматных рецепторах нормализовали работу генов в нейронах и устраняли локализацию C1Q в синапсах. C1Q — белковый комплекс, участвующий в иммунных реакциях, которые могут разрушать связи между нервными клетками при болезни Альцгеймера.
Авторы работы отмечают, что применяемая в исследовании мышиная модель не полностью воспроизводит болезнь Альцгеймера человека. У людей нейродегенеративная болезнь прогрессирует гораздо медленнее, при этом нельзя исключать влияние окружающей среды, а мыши содержались в лаборатории, относительно изолированной от патогенов. Таким образом, экстраполяция результатов работы на человека требует дополнительных клинических исследований. В то же время исследование подтверждает, что нацеливание на mGluR5 может изменить течение болезни Альцгеймера и поощряет использование аллостерических регуляторов в тестирование на людях.