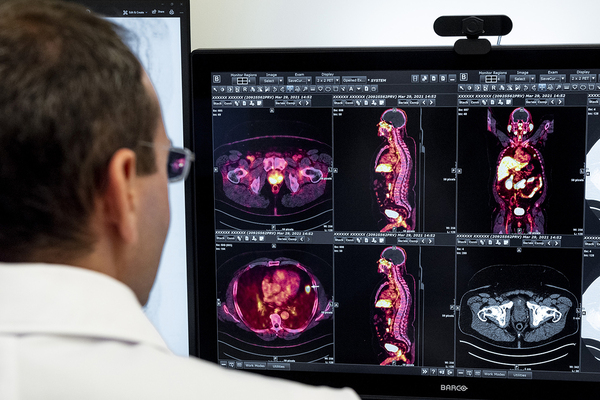
Ученые Московского государственного университета совместно с зарубежными коллегами из Китая и Швеции обнаружили новый механизм, который помогает раковым клеткам избегать гибели от лекарственных препаратов. Оказалось, что недостаток кислорода, возникающий в условиях быстрорастущей опухоли, подавляет апоптоз — программируемую клеточную смерть. Подробно об исследовании, опубликованном в журнале Chemico-Biological Interactions, рассказывает «Лента.ру».
Полезная смерть
Апоптоз — один из важнейших процессов, происходящих в живом организме. Другое его название — программируемая клеточная смерть, и именно это отличает апоптоз от другого типа клеточной гибели — нерегулируемого некроза, который сопровождается воспалительными процессами и может быть вредным и даже смертельным для организма. При апоптозе клетка распадается на фрагменты, которые поглощаются фагоцитами или другими клетками, при этом воспаления не происходит. Апоптоз помогает избавляться от дефектных и мутантных клеток, предотвращает распространение инфекции и участвует в формировании тканей. Согласно одной из теорий старения, апоптоз поддерживает молодость органов, очищая их от старых клеток, и с возрастом программируемая клеточная смерть начинает подавляться.
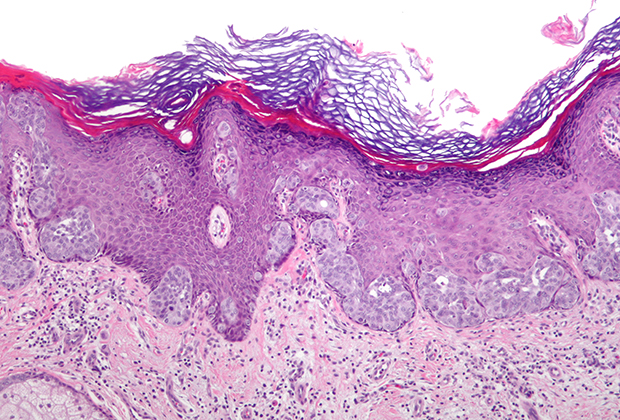
Клетки карциномы
Фото: Википедия
Апоптоз помогает уничтожать и опухолевые клетки. Поэтому избегание апоптоза — одна из характерных особенностей растущих опухолевых тканей. Многие исследовательские коллективы уже наблюдали, что подавление программируемой клеточной смерти происходит в условиях гипоксии или кислородного дефицита. Быстрорастущие опухолевые клетки легко становятся гипоксичными из-за того, что кровеносная система просто не способна доставить к ним достаточно кислорода.
Когда нет кислорода
Из-за гипоксии подавляется митохондриальное окислительное фосфорилирование. Митохондрии обеспечивают процесс клеточного дыхания, а окислительное фосфорилирование, происходящее в них, задействует кислород, чтобы производить молекулы АТФ, обеспечивающие клетки энергией для важных химических реакций. В условиях гипоксии клетки адаптируются к низкому уровню кислорода за счет стабилизации индуцируемого гипоксией фактора (HIF).
HIF — это молекулы, которые реагируют на недостаток кислорода в клеточной среде, меняя экспрессию генов. Известно, что эти факторы связаны с резистентностью опухолей к терапии, образованию метастазов и низкой выживаемостью пациентов. HIF индуцирует гены, которые контролируют важные элементы биологии рака, включая ангиогенез (формирование новых кровеносных сосудов), выживаемость клеток, усвоение глюкозы и инвазию мигрирующих опухолевых клеток, приводящую к появлению новых очагов.
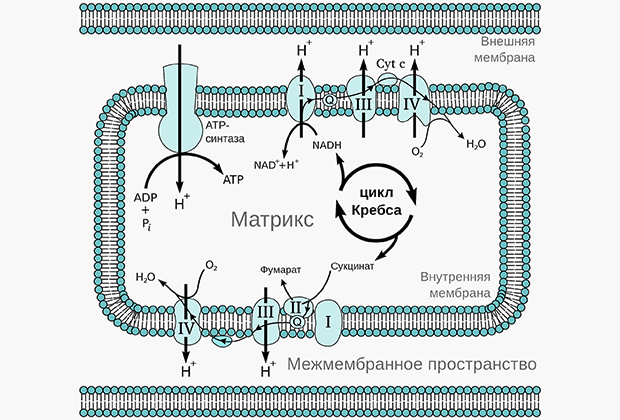
Окислительное фосфорилирование в митохондриях
Изображение: Fvasconcellos / Википедия
В частности, HIF стимулирует ключевые этапы гликолиза, основного пути усвоения клеткой глюкозы. Он катализирует первую реакцию гликолиза — фосфорилирование молекулы сахара. В результате происходит роковой метаболический сдвиг, который усиливает производство энергии в виде АТФ в обход митохондрий. Вместо того чтобы пируват (продукт расщепления сахара в ходе гликолиза) окислялся в митохондриях, он конвертируется в лактат. Кроме того, стабилизация транскрипционных факторов приводит к подавлению активности митохондрий, и заодно апоптоза, который запускают эти органеллы.
Еще один игрок
Другим важным регулятором клеточной гибели является фактор транскрипции p53. Он регулирует экспрессию различных способствующих апоптозу белков Bcl-2 и приводит к образованию пор во внешней мембране митохондрий, запуская тем самым ключевой митохондриальный апоптотический путь. Из митохондрий выходит важный белковый комплекс цитохрома с, который выходит в цитозоль клетки и формирует апоптосомы, запускающие каскад апоптозных реакций. Важную роль в увеличении проницаемости митохондриальной мембраны играют активные формы кислорода (АФК), которые образуются как побочные продукты окислительного фосфорилирования. Однако при подавлении митохондриальной активности генерация АФК также тормозится.
Во многих опухолях ген р53 либо мутирован, либо его экспрессия подавлена. Считается, что взаимодействие между HIF и белками семейства p53 может быть определяющим фактором прогрессирования рака. В то же время связь между гипоксией и подавлением p53 оставалась спорной.
Последний кусок мозаики
В новом исследовании авторы доказали, что пониженный уровень кислорода в опухолевых тканях действительно ослабляет активность генов, кодирующих p53, что, в свою очередь, приводит к подавлению апоптотических белков Bax, Bid и Puma. Из-за этого в мембране митохондрий плохо образуются поры, мешая запуску программируемой клеточной гибели.
В ходе эксперимента специалисты использовали дефероксамин (ДФО), который широко применяется для имитации гипоксии. Сначала ученые проверили, действительно ли ДФО вызывает гипоксию в клетках карциномы толстой кишки человека, наблюдая за уровнем HIF. Выяснилось, что уровень индуцируемого гипоксией фактора вырастает через восемь часов после обработки. Имитация условий гипоксии приводила к ослаблению потребления кислорода митохондриями.
Исследователи оценили, насколько раковые клетки, страдающие от гипоксии, восприимчивы к традиционным противораковым препаратам доксорубицину и цисплатину. Доксорубицин повреждает ДНК через вставку алкильной группы и может приводить к образованию двухцепочечных разрывов ДНК, тогда как цисплатин перекрестно связывает пуриновые основания, блокируя деление клеток, и приводит к апоптозной гибели клеток. Оказалось, что одновременное применение противораковых препаратов и ДФО значительно уменьшало апоптоз. При сочетании противораковых препаратов с ДФО уменьшался уровень способствующих апоптозу белков Bax, Bid и Puma. Экспрессия регулирующего их активность гена p53 также снижалась при имитации гипоксических условий.
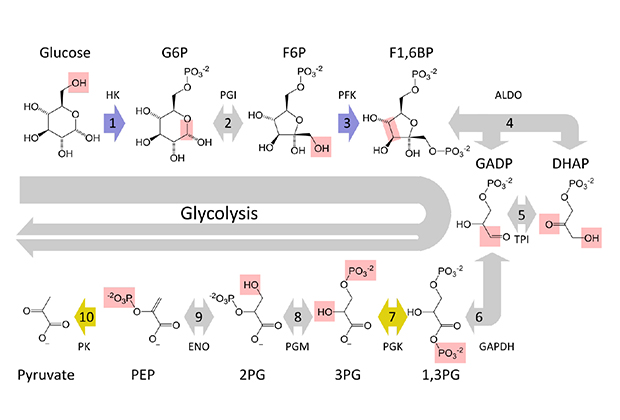
Путь гликолиза
Изображение: Thomas Shafee / Википедия
И, наконец, ученые поместили клетки в настоящие гипоксические условия — в инкубатор, где концентрация кислорода поддерживалась на уровне 0,1 процента в течение 24 часов. Их также обрабатывали доксорубицином и цисплатином, а оценку апоптоза проводили в конце следующих 24 часов. Недостаток кислорода подавлял апоптоз, уменьшал уровень р53 и проапоптотического белка Puma. Аналогичные эксперименты с мутантными раковыми клетками, у которых отсутствовал р53, показали, что эти клетки особо устойчивы к факторам, вызывающим апоптоз.
***
Поскольку в опухолевых клетках p53 часто мутирован, попытки повысить его активность ни к чему не приведут. К счастью, в клетках предусмотрены независимые пути активации апоптоза, на которые можно повлиять препаратами. Например, таким средством является альфа-токоферол сукцинат, который преодолевает устойчивость к лечению клеток нейробластомы (детской разновидности рака мозга) в условиях гипоксии. Кроме того, свою роль могут сыграть и рибосомные белки, которые могут активировать механизмы остановки клеточного цикла или апоптоз.
Рак — очень сложное заболевание, которое способно избегать лекарственную терапию и развивать устойчивость к ней разными способами. Однако ученые не только с каждым разом лучше понимают механизмы возникновения этой устойчивости, но и обнаруживают все больше и больше уязвимых точек, которые позволяют сдерживать рак и повышать выживаемость пациентов. В любом случае чем раньше начато лечение, тем больше вероятность остановить рост опухоли.